Die Dichte
Die Dichte ist eine physikalische Größe und ist definiert als Quotient aus Masse und Volumen eines Stoffes.
Beliebteste Videos
Jetzt mit Spaß die Noten verbessern
und sofort Zugriff auf alle Inhalte erhalten!
30 Tage kostenlos testenInhaltsverzeichnis zum Thema
- Dichte in der Schule und der Lebenswelt
- Dichtebestimmung von Feststoffen
- Dichte von Flüssigkeiten und Gasen
- Typische Dichten auf, um und in der Erde
- Dichten von Stoffgemischen
Dichte in der Schule und der Lebenswelt
In den Klassenstufen 5 bis 8 wird zunächst die Dichte als Größe in Physik und Chemie eingeführt. In der 9.-13. Klasse erfährt man etwas über Abhängigkeit der Dichte von Temperatur und Druck und zur Bestimmung der Dichte von Flüssigkeiten und Gasen.
Man kennt das Wort Dichte von dem Adjektiv dicht. In „dicht gepackt“ ist es ein Ausdruck dafür, dass sich viel an einem kleinen Ort befindet. Die physikalische Dichte $\varrho$ gibt an, wie viel Masse $m$ in g oder kg in einem Volumen $V$ in cm³ oder m³ vorhanden ist.
Die Dichte ist damit der Quotient aus Masse und Volumen eines Stoffes.
$\varrho= \frac{m}{V}$
Um die Dichte einfacher vergleichen zu können, vereinheitlicht man den Volumenanteil der Dichte. So besitzt die Dichte zumeist nur wenige zusammengesetzte Einheiten:
$[\varrho]=1 \frac{g}{cm^3}=1 \frac{g}{mL}= 1 \frac{kg}{L}=1000 \frac{kg}{m^3}$.
Dichtebestimmung von Feststoffen
Feststoffe besitzen im Vergleich zu Flüssigkeiten und Gasen eine hohe Dichte. Bei regelmäßigen Körpern wie einem Würfel kann das Volumen und damit die Dichte recht leicht bestimmt werden. Das Volumen eines Würfels errechnet sich durch die Multiplikation aller 3 Seitenlängen, also Höhe mal Breite mal Länge. Da bei einem Würfel alle Seiten gleich lang sind, kann man es vereinfachen zu Seitenlänge $a$ hoch 3.
$V_\text{Würfel}=a^3$
Für die Bestimmung der Masse brauchst du natürlich eine Waage. Der Rest ist Einsetzen in die Formel.

Bei unregelmäßigen Körpern ist es aber etwas komplizierter. Eine Methode zur Volumenmessung von unregelmäßigen Körpern erfand Archimedes . Wenn ein Körper komplett in eine Flüssigkeit getaucht wird, verdrängt er genau sein eigenes Volumen an Wasser. Auf diese Weise kann man z.B. herausfinden, ob ein Gegenstand aus purem Gold oder nur vergoldet ist, da Gold eine spezifische Dichte aufweist.
Dichte von Flüssigkeiten und Gasen
Natürlich besitzen auch Flüssigkeiten und Gase eine Dichte. Diese physikalische Größe ist eine Stoffkonstante, die abhängig ist von der Temperatur und dem Druck ist. Flüssigkeiten besitzen keine feste Form. Sie nehmen die Form des Gefäßes an, in dem sie sich befinden. Darüber kann man auch ihr Volumen einstellen. Die Dichte von Flüssigkeiten kann wie folgt gemessen werden. Man gibt eine Flüssigkeit in ein Gefäß, auf dem das Volumen abgelesen werden kann.
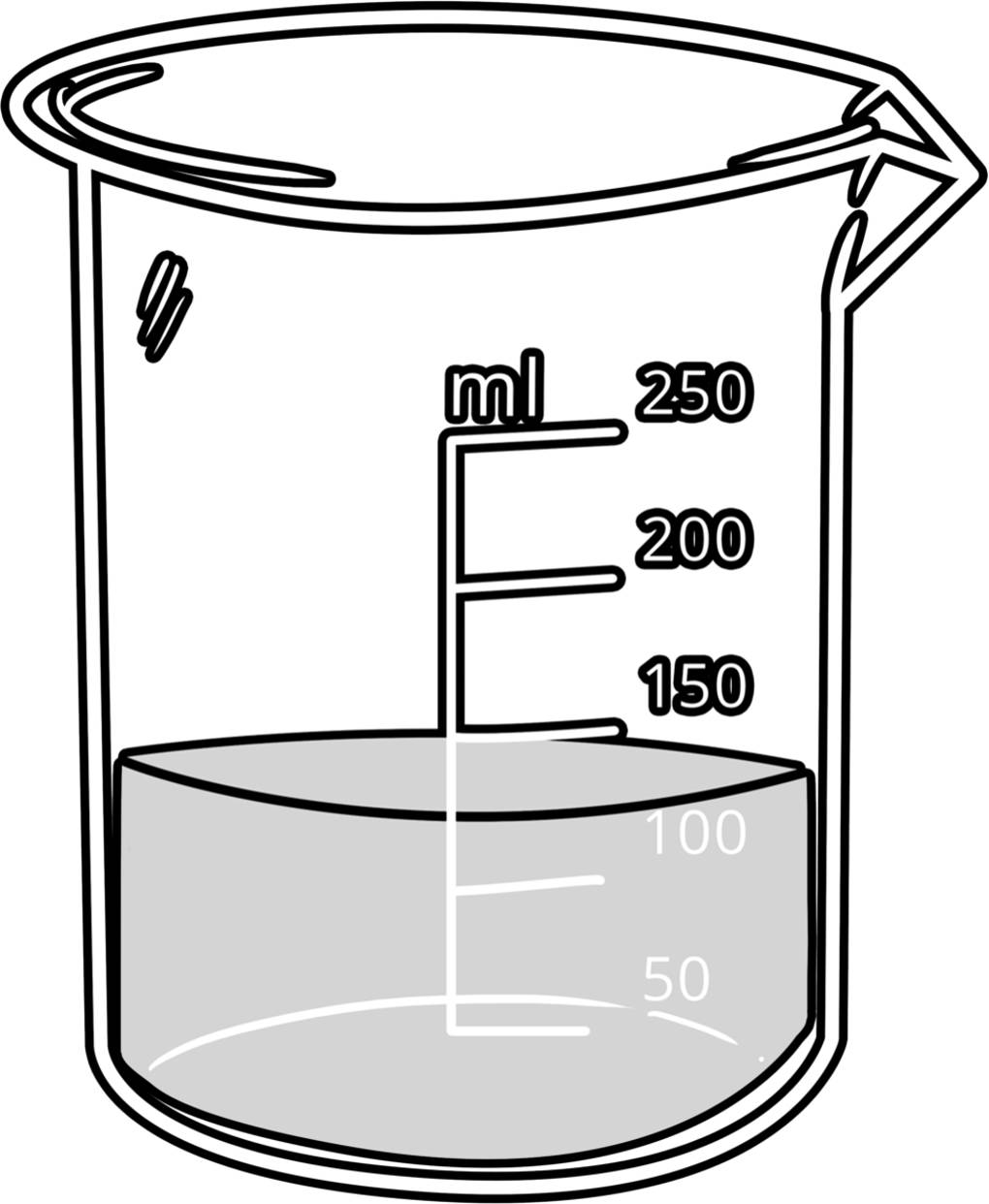
Vorher muss dieses Gefäß gewogen werden. Das Gefäß wird dann samt Inhalt gewogen. Um nun die Masse der Flüssigkeit zu erhalten, musst du die Masse des Gefäßes von der Gesamtmasse abziehen. Es fehlt nur noch das Volumen, welches du am Gefäß ablesen kannst. Setze beide Größen nun in die Formel der Dichte ein und du erhältst die Dichte der gemessenen Flüssigkeit und kannst damit z.B. bestimmen, um welchen Stoff es sich handelt. Gase haben weder eine feste Form, noch ein festes Volumen. Ihr Volumen ist nicht nur von der Temperatur, sondern auch vom Druck abhängig. Die Dichten von Gasen sind recht klein. Für die Berechnung des Volumens und anderen Größen für Gase bedient man sich des idealen Gasgesetzes.
$p\cdot~V=n\cdot~R\cdot~T$
Typische Dichten auf, um und in der Erde
Auch im Umfeld der Erde gibt es Extreme Dichten. Die Luft unserer Atmosphäre zeigt eine eher geringe Dichte von nur:
$\varrho_\text{Luft}=1,2041 \frac{kg}{m^{3}}~~| \text{bei 1013 mbar, 20°C und Meereshöhe}$.
Die größten Dichten finden wir bei den Dichten der Metalle. Diese werden eingeteilt in:
- Leichtmetalle mit $500$ bis $5000 \frac{kg}{m^{3}}$,
- „leichte“ Schwermetalle mit $5001$ bis $10000 \frac{kg}{m^{3}}$,
- „schwere“ Schwermetalle mit $10001$ bis $15000 \frac{kg}{m^{3}}$ und
- „sehr schwere“ Schwermetalle mit $15001$ bis $25000 \frac{kg}{m^{3}}$.
Dichten von Stoffgemischen
Es gibt natürlich auch Stoffgemische. Um die Dichte eines Stoffgemisches zu bestimmen, müssen die Dichten der einzelnen Stoffkomponenten anhand ihrer Volumenverhältnisse addiert werden.
Alle Videos zum Thema
Videos zum Thema
Die Dichte (5 Videos)
Alle Arbeitsblätter zum Thema
Arbeitsblätter zum Thema
Die Dichte (3 Arbeitsblätter)
Beliebteste Themen in Chemie
- Periodensystem
- Ammoniak Verwendung
- Entropie
- Salzsäure Steckbrief
- Kupfer
- Stickstoff
- Glucose Und Fructose
- Salpetersäure
- Redoxreaktion
- Schwefelsäure
- Natronlauge
- Graphit
- Legierungen
- Dipol
- Molare Masse, Stoffmenge
- Sauerstoff
- Elektrolyse
- Bor
- Alkane
- Verbrennung Alkane
- Chlor
- Elektronegativität
- Tenside
- Toluol, Toluol Herstellung
- Wasserstoffbrückenbindung
- Fraktionierte Destillation Von Erdöl
- Carbonsäure
- Ester
- Harnstoff, Kohlensäure
- Reaktionsgleichung Aufstellen
- Redoxreaktion Übungen
- Stärke und Cellulose Chemie
- Süßwasser und Salzwasser
- Katalysator
- Ether
- Primärer Alkohol, Sekundärer Alkohol, Tertiärer Alkohol
- Van-der-Waals-Kräfte
- Oktettregel
- Kohlenstoffdioxid, Kohlenstoffmonoxid, Oxide
- Alfred Nobel
- Wassermolekül
- Ionenbindung
- Phosphor
- Saccharose Und Maltose
- Aldehyde
- Kohlenwasserstoff
- Kovalente Bindung
- Wasserhärte
- Peptidbindung
- Fermentation









 Die Dichte – eine Stoffkonstante
Die Dichte – eine Stoffkonstante
 Bestimmung der Dichte von Flüssigkeiten
Bestimmung der Dichte von Flüssigkeiten
 Bestimmung der Dichte von Gasen
Bestimmung der Dichte von Gasen









