Aminosäuren und Eiweiße
Aminosäuren sind durch Amidbindungen verknüpft, Peptide und Proteine (Eiweiße) bestehen aus Aminosäuren.
Beliebteste Videos
Jetzt mit Spaß die Noten verbessern
und sofort Zugriff auf alle Inhalte erhalten!
30 Tage kostenlos testenInhaltsverzeichnis zum Thema
Struktur und Eigenschaften von Aminosäuren
Aminosäuren sind chemische Verbindungen, die sowohl ein Amin als auch eine Carbonsäure sind. Sie enthalten also Amino-Gruppen $(R-NH_2)$ und Carboxyl-Gruppen $(COOH)$.
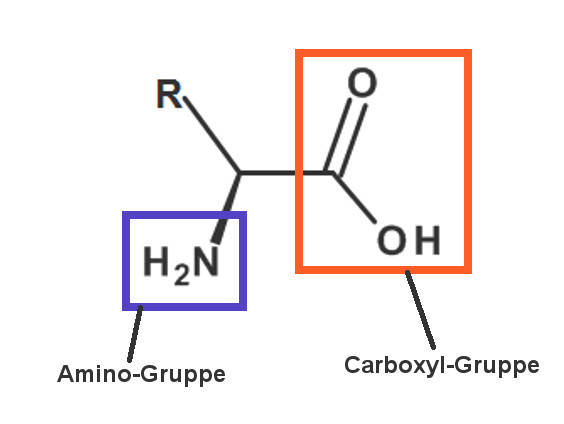
Eine Einteilung der Aminosäuren besteht in der Klassifizierung nach der Stellung der Amino-Gruppe. Je nachdem, an welchem C-Atom von der Carboxyl-Gruppe aus sie sitzen, werden sie als $\alpha$-, $\beta$- oder $\gamma$- Aminosäuren bezeichnet. Die wichtigsten Aminosäuren für uns Lebewesen sind die $\alpha$-Aminosäuren. Die Amino-Gruppe sitzt bei diesen Vertretern am ersten C-Atom nach der Carboxyl-Gruppe. 20 dieser Aminosäuren werden als proteinogene Aminosäuren bezeichnet, da sie die Bausteine aller Proteine darstellen. Einige dieser Aminosäuren können vom menschlichen Körper nicht selbst hergestellt werden. Sie müssen mit der Nahrung aufgenommen werden. Man nennt diese proteinogenen Aminosäuren daher essentielle Aminosäuren.

Für den Menschen gibt es acht essentielle Aminosäuren. Diese sind Isoleucin, Leucin, Lysin, Methionin, Threonin, Tryptophan, Phenylalanin und Valin. $\alpha$-Aminosäuren liegen allesamt bei Raumtemperatur als weiße, kristalline Feststoffe vor.
Das liegt an ihrer Fähigkeit, Zwitterionen auszubilden. Die Carboxyl-Gruppe besitzt ein acides Wasserstoffatom, welches leicht abgegeben werden kann. Die Amino-Gruppe ist in der Lage, ein Proton (Wasserstoffion) aufzunehmen. Es bildet sich eine negative Ladung an der Säure-Gruppe und eine positive Ladung an der Amino-Gruppe. Die Moleküle untereinander können nun durch elektrostatische Kräfte miteinander wechselwirken. Diese Kräfte sind sehr stark und bedingen dadurch einen hohen Schmelzpunkt. Daher sind Aminosäuren Feststoffe. Aminosäuren sind in der Lage, miteinander zu reagieren. Es reagieren die unterschiedlichen Gruppen miteinander und formen die sogenannte Peptidbindung. Dabei wird Wasser abgespalten.
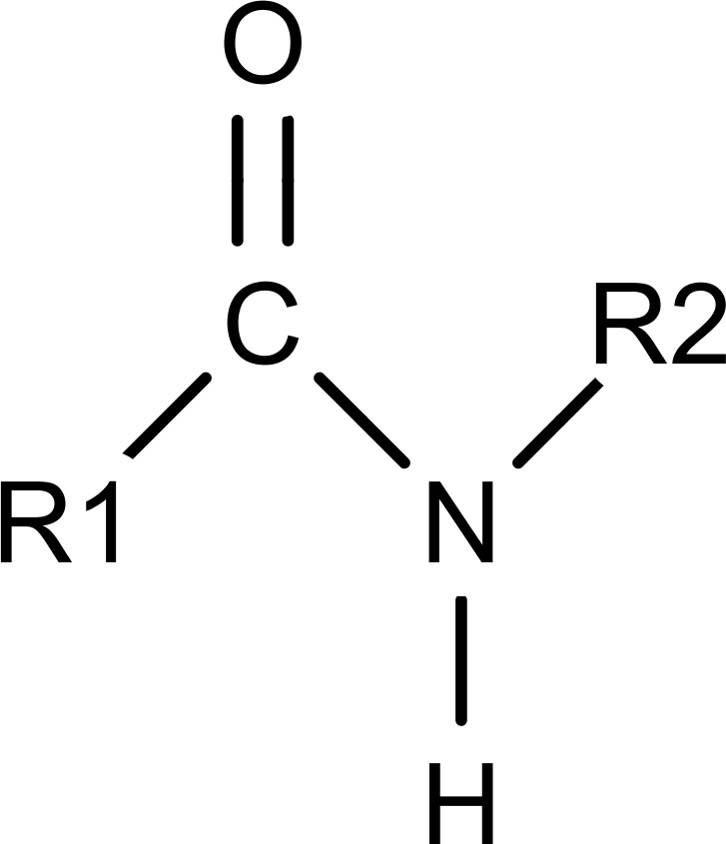
Diese Peptidbindung ist die Grundlage für Eiweiße, da sie es ermöglicht ,Ketten und größere Moleküle mit spezifischen Aufgaben zu bilden.
Proteine und ihr Nachweis
Proteine sind große Makromoleküle, die aus Aminosäuren aufgebaut sind. Sie sind die Bausteine des Lebens. Sehr viele Bestandteile unseres Körpers sind Proteine, so z.B. Muskeln, Haut und Nervengewebe sowie auch Enzyme und Hormone. Mit der Nahrung nehmen wir Proteine zu uns. Diese werden einmal zur Energiegewinnung genutzt, aber auch in ihre Bestandteile zerlegt, die Aminosäuren. In den Zellen gibt es immer einen gewissen Pool an Aminosäuren. Aus diesen können dann, mithilfe des Codes der DNA, neue Proteine zusammengesetzt werden, die der Körper oder die Zelle gerade benötigt. Wichtig bei der Zusammensetzung der Proteine ist die Aminosäuresequenz. Diese ist durch die DNA vorgegeben und beeinflusst das Verhalten und die räumliche Struktur des Proteins. Durch die Ausbildung einer Wasserstoffbrückenbindung ergibt sich die Sekundär- und Quartärstruktur. Sekundär ergibt sich eine Helix- oder Faltblattanordnung. In der Quartärstruktur erhält das Protein seine makromolekulare Form, in der es im Körper wirksam werden kann.
Der Nachweis von Proteinen erfolgt über die Biuretreaktion, bei der eine violette Färbung die Anwesenheit von Eiweißen anzeigt, und die Xanthoproteinreaktion. Hier entsteht durch Zugabe von Salpetersäure eine gelbe Färbung zusammen mit dem Protein.
Enzyme
Viele der lebenswichtigen Stoffwechselprozesse in unserem Körper werden durch Enzyme bewirkt. Diese Enzyme sind Eiweiße, die der Körper selbst herstellt. Enzyme haben einen engen Bereich, in dem sie optimal wirksam sein können. Aus diesem Grund ist es von essentieller Bedeutung, dass der pH-Wert des Blutes und auch die Körpertemperatur innerhalb bestimmter Grenzen verbleiben. Einige Enzyme wirken spezifisch bei bestimmten Stoffen und haben auf andere keine Wirkung. Dies nennt man Substratspezifität. Andere Enzyme sind wirkungsspezifisch. Sie haben eine Aufgabe, wie z.B. die Spaltung von Peptidbindungen, tun dies aber nur, wenn gewisse Komponenten, wie bestimmte Aminosäuren, an den Stellen vorhanden sind.
Alle Videos zum Thema
Videos zum Thema
Aminosäuren und Eiweiße (17 Videos)
Alle Arbeitsblätter zum Thema
Arbeitsblätter zum Thema
Aminosäuren und Eiweiße (13 Arbeitsblätter)
-
 Aminosäuren – Struktur und Eigenschaften
PDF anzeigen
Aminosäuren – Struktur und Eigenschaften
PDF anzeigen -
 Amphoterie am Beispiel von Aminosäuren
PDF anzeigen
Amphoterie am Beispiel von Aminosäuren
PDF anzeigen -
 Aminosäuren – Molekülform in Abhängigkeit vom pH-Wert
PDF anzeigen
Aminosäuren – Molekülform in Abhängigkeit vom pH-Wert
PDF anzeigen -
 Proteinogene und essenzielle Aminosäuren
PDF anzeigen
Proteinogene und essenzielle Aminosäuren
PDF anzeigen -
 Isoelektrischer Punkt
PDF anzeigen
Isoelektrischer Punkt
PDF anzeigen -
 Proteine – Einführung
PDF anzeigen
Proteine – Einführung
PDF anzeigen -
 Nachweis von Proteinen
PDF anzeigen
Nachweis von Proteinen
PDF anzeigen -
 Peptidsynthese
PDF anzeigen
Peptidsynthese
PDF anzeigen -
 Peptidbindung und Primärstruktur
PDF anzeigen
Peptidbindung und Primärstruktur
PDF anzeigen -
 Abbau von Peptidketten
PDF anzeigen
Abbau von Peptidketten
PDF anzeigen -
 Der räumliche Aufbau von Proteinen
PDF anzeigen
Der räumliche Aufbau von Proteinen
PDF anzeigen -
 Proteine und Peptide – Welche Kräfte stabilisieren die Raumstruktur?
PDF anzeigen
Proteine und Peptide – Welche Kräfte stabilisieren die Raumstruktur?
PDF anzeigen -
 Enzyme und ihre Wirkung
PDF anzeigen
Enzyme und ihre Wirkung
PDF anzeigen
Beliebteste Themen in Chemie
- Periodensystem
- Ammoniak Verwendung
- Entropie
- Salzsäure Steckbrief
- Kupfer
- Stickstoff
- Glucose Und Fructose
- Salpetersäure
- Redoxreaktion
- Schwefelsäure
- Natronlauge
- Graphit
- Legierungen
- Dipol
- Molare Masse, Stoffmenge
- Sauerstoff
- Elektrolyse
- Bor
- Alkane
- Verbrennung Alkane
- Chlor
- Elektronegativität
- Tenside
- Toluol, Toluol Herstellung
- Wasserstoffbrückenbindung
- Fraktionierte Destillation Von Erdöl
- Carbonsäure
- Ester
- Harnstoff, Kohlensäure
- Reaktionsgleichung Aufstellen
- Redoxreaktion Übungen
- Stärke und Cellulose Chemie
- Süßwasser und Salzwasser
- Katalysator
- Ether
- Primärer Alkohol, Sekundärer Alkohol, Tertiärer Alkohol
- Van-der-Waals-Kräfte
- Oktettregel
- Kohlenstoffdioxid, Kohlenstoffmonoxid, Oxide
- Alfred Nobel
- Wassermolekül
- Ionenbindung
- Phosphor
- Saccharose Und Maltose
- Aldehyde
- Kohlenwasserstoff
- Kovalente Bindung
- Wasserhärte
- Peptidbindung
- Fermentation
































