Sesselform-Schreibweise der Pyranosen

in nur 12 Minuten? Du willst ganz einfach ein neues
Thema lernen in nur 12 Minuten?
-
 5 Minuten verstehen
5 Minuten verstehen
Unsere Videos erklären Ihrem Kind Themen anschaulich und verständlich.
92%der Schüler*innen hilft sofatutor beim selbstständigen Lernen. -
 5 Minuten üben
5 Minuten üben
Mit Übungen und Lernspielen festigt Ihr Kind das neue Wissen spielerisch.
93%der Schüler*innen haben ihre Noten in mindestens einem Fach verbessert. -
 2 Minuten Fragen stellen
2 Minuten Fragen stellen
Hat Ihr Kind Fragen, kann es diese im Chat oder in der Fragenbox stellen.
94%der Schüler*innen hilft sofatutor beim Verstehen von Unterrichtsinhalten.
Grundlagen zum Thema Sesselform-Schreibweise der Pyranosen
In diesem Video geht es um die Sesselform-Schreibweise für Monosaccharide (speziell Glucose). Dazu werden die Grenzen der Fischer- und der Haworth-Schreibweise beleuchtet und daraus die Notwendigkeit der neuen Schreibweise erklärt. Außerdem werden im Anschluss die verschiedenen Konformationen beschrieben und erläutert.
Transkript Sesselform-Schreibweise der Pyranosen
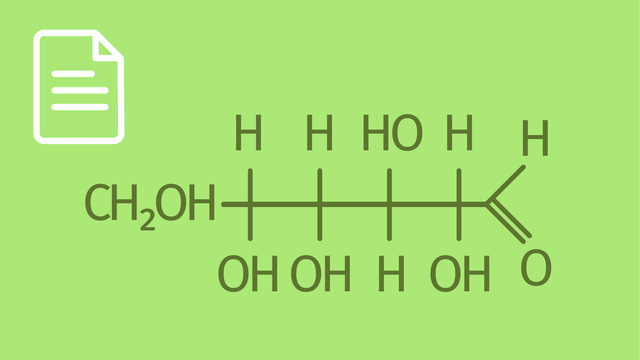
Guten Tag und herzlich willkommen. In diesem Video geht es um die Sesselform-Schreibweise der Pyranosen. Es wäre hilfreich, wenn du über folgende Vorkenntnisse verfügst: Du solltest dich in der Monosaccharidechemie bereits gut auskennen, du solltest wissen, was Pyranosen, Furanosen, D-Ribose und die Ringisomere der D-Ribosen sind. Die Fischer-Projektion und die Haworth-Formeln sind dir gut vertraut. Du weißt, was Anomere sind, weißt, was Cyclohexan ist, die Begriffe Sessel und Wanne sind dir gut bekannt. Du kennst die Begriffe Konstitution, Konfiguration und Konformation eines Moleküls. Ziel des Videos ist es, genauere Vorstellungen über die Konformation der Pyranosen am Beispiel der Glucose zu vermitteln. Das Video habe ich in 6 Abschnitte gegliedert. 1. Die Grenzen der Darstellung nach Fischer und Haworth, 2. Cyclohexan und Sesselform, 3. Stabilität der D-Glucopyranosen, 4. 4C1-Konformation und 1C4-Konformation, 5. Konformationen für Furanosen und 6. Zusammenfassung. 1. Die Grenzen der Darstellung nach Fischer und Haworth. Ich habe hier ein Molekülskelett nach Fischer gezeichnet, das ich nun beschriften möchte. Es handelt sich um eine Aldose. Sie hat eine Aldehytgruppe oben, unten befindet sich eine Hydroxymethylgruppe. An allen anderen Kohlenstoffatomen sitzt jeweils eine Hydroxygruppe. Das ist eine Pyranose nach Fischer, ihr habt sie sicher schon als D-Glucose erkannt. In der Ringform zeichnet man die D-Glucose gerne so. Das ist ein D-Glucosemolekül, präsentiert durch eine Haworth-Formel. Ich beschrifte nun die einzelnen Kohlenstoffatome mit den Ziffern 1-6, um zu sehen, wo sie sich nach der Zyklisierung befinden. Es ist offensichtlich, wofür die Darstellungsweisen nach Fischer und Haworth Verwendung finden. Die Fischerprojektion verwendet man für die Darstellung einer Kette, die Haworth-Formel wird für die Darstellung des Rings verwendet. Die Haworth-Formel gibt sowohl Konstitution als auch Konfiguration des D-Glucosemoleküls in der Ringform an. Es wird aber keine Aussage über die Konformation des Moleküls geliefert. Bei dem Molekül in Ringform handelt es sich um β-D-Glucose. Das erkennt man daran, dass die Hydroxygruppe am anomeren Kohlenstoffatom 1 nach oben zeigt. Wie ist nun aber auch die Konformation des β-D-Glucosemoleküls darstellbar? 2. Cyclohexan und Sesselform. Cyclohexan hat die Summenformel C6H12. In Ringschreibweise wird es so dargestellt, das wäre die entsprechende Haworth-Formel. Wir wissen aber auch, dass das Cyclohexanmolekül vorzugsweise in Sesselform auftritt. Außerdem ist bekannt, dass der Sessel stabiler als die Wanne ist. Wenn wir ein Kohlenstoffatom des Ringes durch ein Sauerstoffatom substituieren und ein Wasserstoffatom durch eine Hydroxygruppe, dann erhalten wir folgendes Molekül. Wir erhalten die Grundstruktur des Pyranose-Rings und somit die Konformation der Pyranose. Damit verfügen wir über eine komplette Vorstellung der Struktur des Moleküls. 3. Stabilität der D-Glucopyranosen. Hier habe ich das Grundgerüst der D-Glucopyranose gezeichnet, mit den Bindungen zu den entsprechenden Substituenten. Die Hydroxymethylgruppe befindet sich hier. Die verbleibenden Hydroxygruppen und entsprechend die Wasserstoffatome müssen mit großer Sorgfalt eingezeichnet werden. Am Kohlenstoffatom ganz rechts, am sogenannten anomeren Kohlenstoffatom habe ich nun wieder 2 Möglichkeiten, die Hydroxygruppe und das entsprechende Wasserstoffatom anzuordnen. Ich habe mich dafür entschieden, dass die Hydroxygruppe nach unten zeigt. Damit handelt es sich um α-D-Glucopyranose. Mit der Vorgabe links kann ich nun das andere Isomer der D-Glucopyranose zeichnen. Die Hydroxygruppe zeigt hier zur Seite. Das ist das Molekül der β-D-Glucopyranose. Wir erinnern uns der Begriffe äquatorial und axial in Bezug auf die Sesselform des Cyclohexans. Die unterschiedlichen Positionen der Substituenten möchte ich nun hier eintragen. An die Hydroxygruppen, die direkt mit dem Ring verknüpft sind, schreibe ich jeweils ein kleines e, am anomeren Kohlenstoffatom schreibe ich an die Hydroxygruppe ein a, denn sie ist anders bezüglich des Ringes ausgerichtet. Das kleine e bedeutet, dass die entsprechenden Hydroxygruppen eine äquatoriale Lage bezüglich des Rings aufweisen. Wir wissen aber auch, dass diese äquatoriale Anordnung zu einer Stabilisierung des Moleküls führt. Wenn eine Ausrichtung nach a, das heißt axial, vorliegt, so wird für manche Moleküle eine Stabilisierung hervorgerufen. Wir sprechen dann vom anomeren Effekt. 4. 4C1- und 1C4-Konformationen. Das Molekül der α-D-Glucopyranose habe ich noch ein Mal stehen lassen und lösche nun die Wasserstoffatome, die sich am Ring befinden, fort. Für die Betrachtung der genannten Konformationen sind die Kohlenstoffatome 4 und 1 von Bedeutung. Die Konformation, die hier die α-D-Glucopyranose aufweist, bezeichnet man als 4C1-Konformation. Im Gegensatz zum Cyclohexansessel kann der Pyranosesessel auch eine andere Konformation aufweisen. Die Hydroxymethylgruppe und die Hydroxygruppen, die sich am Ring befinden, muss ich nun exakt einzeichnen. Bei diesem Molekül handelt es sich ebenfalls um eine Glucopyranose, es ist aber die α-L-Glucopyranose. Wir markieren die Kohlenstoffatome 1 und 4. Eine derartige Konformation wird als 1C4-Konformation bezeichnet. Die Moleküle links und rechts bilden zusammen ein Enantiomerenpaar. Sind die Hydroxygruppen am anomeren Kohlenstoffatom 1 nicht axial, sondern äquatorial gerichtet, so bezeichnet man die entsprechenden Verbindungen als β-D-Glucopyranose bzw. β-L-Glucopyranose. In Abschnitt 5 müssen wir eine kleine aber wichtige Frage klären. Wie sieht die Sesselform für Furanosen aus? Wir erinnern uns, dass das Tetrahydrofuranmolekül das Grundgerüst für Furanosen ist. Als Beispiel für eine Furanose habe ich hier die α-D-Ribofuranose gewählt. Das Molekül dieses Monosaccharids wurde hier durch die Haworth-Formel dargestellt. Man muss wissen, dass die α-D-Ribofuranose mehrere Konformere ausbildet. Diese sind energetisch sehr ähnlich und gehen leicht ineinander über. Somit ist es nicht sinnvoll, die Sesselschreibweise für das Molekül der α-D-Ribofuranose zu wählen. 6. Zusammenfassung. Wir haben bereits früher gelernt, dass Monosaccharide als offenkettige Verbindungen vorliegen können. Hier haben wir die Kette der D-Glucose, die in Fischerprojektion dargestellt wird. Wir wissen aber auch, dass ein Monosaccharid als Ring vorliegen kann. In diesem Fall soll es sich um das β-Anomer handeln. Wichtige Struktureigenschaften dieses Moleküls werden durch die Haworth-Formel vermittelt. Wir erhalten Informationen über seine Konstitution und Konfiguration. Aber erst die Sesselformschreibweise, die von der Struktur des Cyclohexanmoleküls abgeleitet ist, liefert ein tieferes Verständnis für die Struktur dieses Moleküls. Im Unterschied zur Haworth-Formel liefert die Sesselformschreibweise zusätzliche Informationen über die Konformation des Moleküls. Im Gegensatz zum Cyclohexan kann der Sessel bei den Pyranosen auf 2 Arten ausgebildet sein. Zum einen ist das die 4C1-Konformation. Eine solche Konformation besitzen die Moleküle der D-Reihe. Die zweite Konformation ist die 1C4-Konformation. Diese Konformation besitzen die Moleküle der L-Reihe. Beide Moleküle bilden zusammen ein Enantiomerenpaar. Die Struktur der Furanosen wird sinnvoll durch die Haworth-Formeln dargestellt. Die Furanosen besitzen in der Ringform verschiedenen Konformere von etwa gleicher Energie. Daher ist es nicht sinnvoll, die Sesselformschreibweise für Furanosen zu wählen. Die Haworth-Formel ist hier die Methode der Wahl. Ich danke für die Aufmerksamkeit, alles Gute. Auf Wiedersehen.
Sesselform-Schreibweise der Pyranosen Übung
-
Nenne die Namen und Merkmale verschiedener Darstellungsformen von Zuckern.
TippsDie Fischer-Projektion wird vorzugsweise für die Darstellung der Kettenform von Monosacchariden verwendet.
Die Haworth-Projektion zeigt grob an, wie die Hydroxygruppen ausgerichtet sind.
Die Sesselform-Darstellung stellt das Molekül am realistischsten dar.
LösungAls Beispiel für ein Monosaccharid wurde die $\alpha$-D-Glucose gewählt.
Fischer-Projektion
Die Fischer-Projektion liefert die Darstellung für das Glucose-Molekül in Kettenform. Die Struktur wird dabei als völlig planar angenommen. Im Unterschied zum Ring handelt es sich beim Ketten-Molekül um einen Aldehyd. Man sagt, dass die $-OH$-Gruppen am Kohlenstoff-Skelett (der Kette) „links“ und „rechts“ angeordnet sind.Haworth-Formel
Die Haworth-Formel ist eine schematisch vereinfachte Darstellung des Glucose-Moleküls in Ringform. Der Ring wird dabei planar gezeichnet. Man sagt, dass die $-OH$-Gruppen „oben“ und „unten“ am Sechsring angeordnet sind.Sessel-Struktur
Die Sesselform-Schreibweise des Glucose-Moleküls ist die korrekte räumliche Darstellung der Struktur des Monosaccharids in Ringform. Der Ring wird realistisch räumlich gezeichnet. Die Schreibweise gibt die Konformation korrekt wieder. Bei den $-OH$-Gruppen am Sechsring unterscheidet man zwischen „axialer“ und „äquatorialer“ Anordnung. -
Nenne Vorteile und Grenzen der Darstellung nach Haworth.
TippsVereinfachungen sind häufig nützlich. Für bestimmte Anwendungen besitzen sie Grenzen.
LösungDie Haworth-Darstellung bietet einige Vorteile:
Die Verknüpfungen zwischen den Atomen werden korrekt dargestellt. Man kann gut erkennen, welche Atome mit welchen Atomen verbunden sind. Man erkennt einen Sechsring, bestehend aus fünf Kohlenstoffatomen und einem Sauerstoffatom. Außerdem wird auch die Konstitution korrekt dargestellt. Das bedeutet die Kenntnis der einzelnen Verknüpfungen zwischen den Atomen.
Die Konformation wird allerdings nicht exakt abgebildet, denn dann müsste man den Sessel erkennen, was in der Darstellung nach Harworth nicht möglich ist. Nachteilig an dieser Darstellung ist also, dass der Sechsring im Molekül planar dargestellt wird.
-
Benenne die folgenden Zucker.
TippsManche Hexosen bilden nur ungern Fünfringe.
Maltose entsteht aus Stärke.
Lösung$\alpha$-D-Glucose
Die Darstellung zeigt die Sesselform. Das $\alpha$-Isomer ist an der Stellung der Hydroxygruppe in 1-Stellung (ganz rechts) zu erkennen. Sie zeigt nach unten.$\beta$-D-Glucose
In der Haworth-Formel sieht man sehr gut, dass die Hydroxygruppe in 1-Stellung nach oben zeigt. Daher handelt es sich um das $\beta$-Isomer.$\beta$-D-Fructose
Die Hexose (6 Kohlenstoffatome) ist zu erkennen. Das Monosaccharid ist befähigt, einen Fünfring zu bilden. Die Glucosen vermögen das nicht.Saccharose
Das Molekül ist aus den Monosacchariden Glucose und Fructose aufgebaut.Maltose
Das ist Malzzucker. Ein Molekül dieses Disaccharids besteht aus zwei Glucose-Molekülen.D-Ribose
Die Keilstrichformel ist etwas gewöhnungsbedürftig. Man kann allerdings auszählen, dass es sich bei diesem Zucker um eine Pentose (5 Kohlenstoffatome) handelt. Die übrigen genannten Zucker sind Hexosen. -
Vergleiche die verschiedenen Darstellungen von $\alpha$-D-Glucose.
TippsDie Stereochemie lässt sich nur aus anachronistischen Darstellungen nicht herauslesen.
LösungNamen der Darstellungsformen
Darstellung 1 : Fischer-Projektion
Das ist eine historische Darstellung. Die stereochemische Aussage ist nicht korrekt. Traditionell wird diese Darstellung nach wie vor weit verwendet. Sinnvollerweise werden meist nur die Ketten beschrieben.Darstellung 2 : Haworth-Formel
Diese Formel wird ausschließlich für die Darstellung von Ringen verwendet. Sie zeigt grob an, welche Hydroxy-Gruppe „nach oben“ und welche „nach unten “ zeigt. Die Vermittlung adäquater räumlicher Strukturverhältnisse ist begrenzt.Darstellung 3 : Sesselform-Schreibweise
Der Sessel ist ein Strukturmerkmal des Sechsrings. Daher werden nur Ringe abgebildet. Es wird eine bessere räumliche Darstellung des Moleküls als durch die Haworth-Projektion vermittelt.Darstellung 4 : Keilschriftformel
Die Verwendung erfolgt meist für die Darstellung der Kette. Der visuelle Zugang zur räumlichen Darstellung des Ringes ist begrenzt. Eine korrekte stereochemische Zuordnung aller Kohlenstoffatome ist problemlos möglich.Räumliche Darstellung
Nach der ausführlichen Beschreibung der vier Darstellungsformen ist es nicht mehr schwer, sie nach aufsteigender Qualität zu ordnen:
1 < 4 < 2 < 3
Stereochemie
Das Glucose-Molekül enthält mehrere asymmetrische Kohlenstoffatome (vier verschiedene Substituenten). Die Zuordnung zu den räumlichen Anordnungen R oder S liefern nur Darstellungen, die ein korrektes Abbild der Wirklichkeit liefern. Die historische Fischer-Projektion erfüllt diese Bedingung nicht. Hauptkritikpunkt dieser Darstellung ist die Interpretation des Moleküls nicht als Zickzack-Kette, sondern als unrealistisch gewölbtes Gebilde.
- Darstellung 1 : nicht möglich
- Darstellung 2 : möglich
- Darstellung 3 : möglich
- Darstellung 4 : möglich
-
Erkenne die Sesselform-Schreibweise für Pyranosen.
TippsDu musst unterscheiden zwischen der Fischer-Projektion, den Haworth-Formeln und der Sesselform-Schreibweise.
Verwechsle bitte nicht die Sessel-Struktur mit der Wannen-Struktur.
LösungWir betrachten die Strukturformeln einzeln von links nach rechts.
- Nein, es handelt sich um eine Kettenstruktur in Fischer-Projektion.
- Nein, es handelt sich hier um eine Haworth-Formel.
- Ja, das ist eine Pyranose in Sesselform.
- Nein, das ist eine Furanose in der Haworth-Projektion.
- Nein, wir haben es hier mit einer Kette in Fischer-Projektion zu tun.
- Nein, das ist keine Sessel-Struktur. Zwar handelt es sich um eine korrekte Darstellung der Konformation (Geometrie des Moleküls). Allerdings wird in der Abbildung die Struktur einer Wanne gezeigt.
-
Bestimme die stereochemische Zuordnung der Kohlenstoffatome in einem Glucose-Molekül.
TippsKohlenstoffatome mit vier unterschiedlichen Substituenten sind chiral. Anderenfalls sind die Kohlenstoffatome achiral.
Lösung- H(O=)C[1]- ist achiral: Das Carbonyl-Sauerstoffatom schafft zwei identische Bindungen („Substituenten“). Daher ist das Kohlenstoffatom nicht chiral.
- -C[2](OH)H- ist chiral: Vier verschiedene Substituenten: H, OH und zwei verschiedene organische Reste.
- -(HO)HC[3]- ist chiral: Vier verschiedene Substituenten: H, OH und zwei verschiedene organische Reste.
- -C[4](OH)H- ist chiral: Vier verschiedene Substituenten: H, OH und zwei verschiedene organische Reste.
- -H(HO)C[5]- ist chiral: Vier verschiedene Substituenten*: H, OH und zwei verschiedene organische Reste.*
- HO-C[6]$H_2$- ist achiral: Zwei Substituenten, die Wasserstoffatome, sind gleich. Damit ist das Kohlenstoffatom nicht chiral.

Grundbaustoffe der Nahrung – Kohlenhydrate, Eiweiße und Fette

Monosaccharide

Glucose und Fructose

Glucose – Kette oder Ring?

Monosaccharide mit 3 bis 6 C-Atomen

Monosaccharide – Nomenklatur und Stereochemie

Monosaccharide – Eigenschaften und Reaktionen

Pyranosen und Furanosen

D-Ribopyranose und D-Ribofuranose

Sesselform-Schreibweise der Pyranosen

Halbacetal- und Acetalbildung

Disaccharide

Disaccharide – Besondere Glykoside

Reduzierende und nichtreduzierende Disaccharide

Saccharose und Maltose

Polysaccharide

Polysaccharide – Cellulose, Stärke, Glykogen

Stärke und Cellulose

Nachweis von Kohlenhydraten

Moleküldarstellungen von Kohlenhydraten

Zuckerderivate
Glykoside und glykosidische Bindung

Glykolipide und Glykoproteine

Hyaluronsäure, Heparin, Chitin
9.178
sofaheld-Level
6.600
vorgefertigte
Vokabeln
8.108
Lernvideos
37.100
Übungen
33.418
Arbeitsblätter
24h
Hilfe von Lehrkräften

Inhalte für alle Fächer und Klassenstufen.
Von Expert*innen erstellt und angepasst an die Lehrpläne der Bundesländer.
Testphase jederzeit online beenden
Beliebteste Themen in Chemie
- Periodensystem
- Ammoniak Verwendung
- Entropie
- Salzsäure Steckbrief
- Kupfer
- Stickstoff
- Glucose Und Fructose
- Salpetersäure
- Redoxreaktion
- Schwefelsäure
- Natronlauge
- Graphit
- Legierungen
- Dipol
- Molare Masse, Stoffmenge
- Sauerstoff
- Elektrolyse
- Bor
- Alkane
- Verbrennung Alkane
- Chlor
- Elektronegativität
- Tenside
- Toluol, Toluol Herstellung
- Wasserstoffbrückenbindung
- Fraktionierte Destillation Von Erdöl
- Carbonsäure
- Ester
- Harnstoff, Kohlensäure
- Reaktionsgleichung Aufstellen
- Redoxreaktion Übungen
- Stärke und Cellulose Chemie
- Süßwasser und Salzwasser
- Katalysator
- Ether
- Primärer Alkohol, Sekundärer Alkohol, Tertiärer Alkohol
- Van-der-Waals-Kräfte
- Oktettregel
- Kohlenstoffdioxid, Kohlenstoffmonoxid, Oxide
- Alfred Nobel
- Wassermolekül
- Ionenbindung
- Phosphor
- Saccharose Und Maltose
- Aldehyde
- Kohlenwasserstoff
- Kovalente Bindung
- Wasserhärte
- Peptidbindung
- Fermentation




 5 Minuten verstehen
5 Minuten verstehen
 5 Minuten üben
5 Minuten üben
 2 Minuten Fragen stellen
2 Minuten Fragen stellen

 Bereit für eine echte Prüfung?
Bereit für eine echte Prüfung?












Hallo Herr Otto
Vielleicht hilft es, wenn ich die Zeit nenne. Bei Minute 7:28 würde ich die Nummerierung vertauschen, also 4 und 1. Alles Gute
Liebe Nadine,
ich habe mir das Video noch einmal angeschaut. Ich kann in der Zusammenfassung keinen Unterschied zum Inhalt erkennen.
Kleine Unterschiede in der Darstellung scheinen mir unwesentlich.
Für weiterführende Informationen müsstest du ein Buch über Kohlenhydrate anschauen oder einen Zucker-Chemiker befragen.
Alles Gute
Guten Tag Herr Otto
Sie antworten ja immer so zügig, Sie müssen sich nicht entschuldigen. Vielen Dank.
Ich habe zu Hause ständig eine Störung beim Schauen der Videos. Tut mir leid, kann erst morgen und dann in der zweiten Tageshälfte antworten.
Alles Gute
Ich sehe gerade... in der Zusammenfassung haben Sie die Ziffern vertauscht. Sind beide Varianten möglich? Vielen Dank.